
Nicolas Saucisse, Wilfrid Mazier, Vincent Simon, Daniela Cota et al. dans Cell Reports
Satiété : des neurones aux multiples visages
Collaboration de l’équipe de Daniel Cota (Neurocentre Magendie) avec l’équipe de Giovanni Marsicano (Neurocentre Magendie ) et Xavier Fioramonti (Nutrineuro)
L’obésité représente à ce jour l’un des plus grands fléaux de santé publique à travers le monde. Le manque actuel de stratégies efficaces pour prévenir ou lutter contre le surpoids et l’obésité est dû en grande partie à un défaut de connaissance des mécanismes biologiques qui participent au développement de cette maladie.
Le cerveau est un organe central pour la régulation du poids corporel et, par extension, l’apparition ou la prévention de l’obésité. En effet, dans le cerveau, de nombreux neurones communiquent entre eux et avec le reste de l’organisme pour adapter les apports, le stockage et la dépense d’énergie aux besoins de l’organisme. Dans ce contexte, les neurones à POMC (pro-opiomélanocortine) de l’hypothalamus sont classiquement reconnus comme promoteurs de la satiété.
 Dans un article publié dans Cell Reports, Saucisse et al. ont bloqué mTORC1 (mechanistic target of rapamycin complex 1), un mécanisme intracellulaire de détection d’énergie, et ont montré que l’augmentation de la prise alimentaire qui s’ensuit est due à la modification de l’activité des neurones à POMC dans l’hypothalamus. Ainsi, le blocage de mTORC1 mime un état de carence énergétique, auquel les neurones à POMC répondent en diminuant leur effet pro-satiété.
Dans un article publié dans Cell Reports, Saucisse et al. ont bloqué mTORC1 (mechanistic target of rapamycin complex 1), un mécanisme intracellulaire de détection d’énergie, et ont montré que l’augmentation de la prise alimentaire qui s’ensuit est due à la modification de l’activité des neurones à POMC dans l’hypothalamus. Ainsi, le blocage de mTORC1 mime un état de carence énergétique, auquel les neurones à POMC répondent en diminuant leur effet pro-satiété.
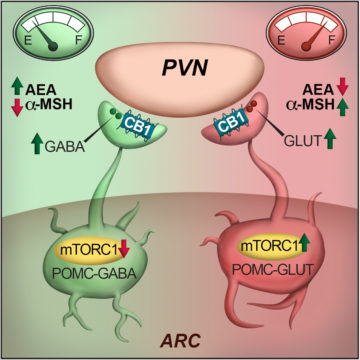
Pour aller plus loin, les auteurs ont découvert que le blocage de mTORC1 avait des effets opposés sur l’activité électrique des neurones à POMC, en fonction du neurotransmetteur produit par ceux-ci. Ils ont ainsi défini des sous-populations de neurones activées ou inhibées par le blocage de mTORC1, dont ils ont caractérisé le profil moléculaire et la distribution spatiale spécifiques dans l’hypothalamus.
Ces résultats démontrent que mTORC1 orchestre l’activité de sous-populations distinctes de neurones à POMC. Les effets opposés du blocage de mTORC1 suggèrent que ces sous-populations pourraient avoir des rôles antagonistes dans la régulation du comportement alimentaire, ce qui remettrait en cause la vision classique des neurones à POMC comme étant uniquement promoteurs de la satiété. De futures études devront clarifier le lien entre l’hétérogénéité des neurones à POMC et leur rôle dans l’obésité, pour le développement de nouvelles stratégies thérapeutiques.
Article
Functional heterogeneity of POMC neurons relies on mTORC1 signaling.
Saucisse N, Mazier W, Simon V, Binder E, Catania C, Bellocchio L, Romanov RA, Léon S, Matias I, Zizzari P, Quarta C, Cannich A, Meece K, Gonzales D, Clark S, Becker JM, Yeo GSH, Fioramonti X, Merkle FT, Wardlaw SL, Harkany T, Massa F, Marsicano G, Cota D.
Cell Rep. 2021 Oct 12;37(2):109800.
doi: 10.1016/j.celrep.2021.109800
Mise à jour: 29/10/21
