Mario Carta et al. dans Nature reviews neuroscience
Mario Carta (IINS), aux côtés de Mikkel Vestergaard (Université de Copenhague) et James. F. A Poulet (MDC et Neuroscience research center, Berlin), ont publié une étude sur la thermosensation.
Comment le cerveau encode les informations thermiques ?
À chaque instant de notre vie, nous sommes plongés dans un environnement dont la température fluctue en permanence. La chaleur du soleil sur notre peau, le contact d’un objet frais ou la douceur d’une boisson froide stimulent continuellement notre cerveau, qui lit et interprète les informations thermiques provenant du monde qui nous entoure. La température constitue un élément fondamental de notre expérience et de notre manière d’interagir avec notre environnement. Pour tous les animaux, elle joue un rôle essentiel dans la modulation des comportements, le choix des habitats et la survie face à des conditions changeantes.
Pourtant, malgré son importance, notre compréhension de la manière dont le cerveau détecte et perçoit la température demeure limitée par rapport à d’autres sens tels que la vision ou l’audition. La majorité des recherches et des revues sur la thermosensation se sont concentrées sur les températures extrêmes douloureuses, celles qui brûlent ou gèlent la peau, ainsi que sur les capteurs moléculaires qui les détectent, comme les canaux ioniques TRP. Beaucoup moins d’attention a été portée à la perception des variations de température non douloureuses, pourtant essentielles pour guider les comportements.
Dans notre revue, nous mettons en lumière les circuits neuronaux et les mécanismes cellulaires qui permettent aux animaux, notamment les rongeurs, les primates (y compris l’humain) et les insects, de détecter et d’interpréter les sensations de chaleur et de fraîcheur non douloureuses. Nous examinons la manière dont ces signaux thermiques sont transmis de la périphérie au cerveau, et comment des motifs distincts d’activité neuronale donnent naissance aux sensations complexes associées à la température. En comparant les mammifères et les insectes, nous révélons des similitudes frappantes, ainsi que des différences importantes, dans la façon dont leurs systèmes nerveux codent et répondent à la température, mettant en évidence des principes de thermosensation conservés au cours de l’évolution.
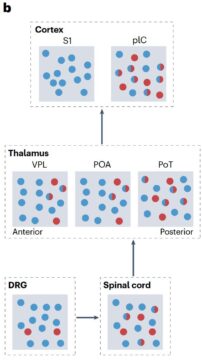
Légende de la figure :
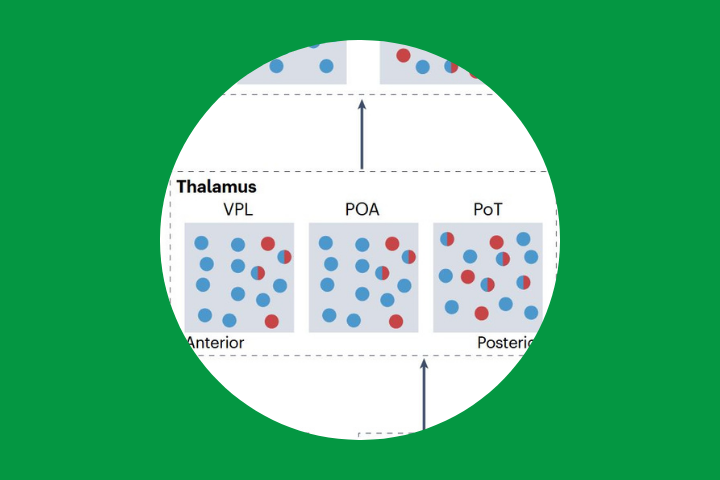
Le réglage thermique cellulaire varie selon les différentes étapes de la voie perceptive. Dans le ganglion de la racine dorsale (GRD), de nombreux neurones sont excités par le froid (cercles bleus), tandis que très peu sont excités par une chaleur non douloureuse (cercles rouges). Cette situation change dans la moelle épinière, où l’on observe davantage de neurones excités par la chaleur ainsi que des neurones à large spectre, activés à la fois par le chaud et le froid (cercles bleus et rouges).
Dans le thalamus, une sensibilité accrue à la chaleur est observée dans les régions postérieures du noyau ventral postérolatéral (VPL) et du noyau postérieur (PO), ainsi que dans le noyau triangulaire postérieur (PoT), tandis que les régions plus antérieures du VPL et du PO présentent une sensibilité prédominante au froid.
Dans le cortex, le cortex somatosensoriel primaire (S1) est principalement sensible au froid, alors que le cortex insulaire postérieur (pIC) contient des neurones sensibles au chaud, au froid, ainsi que des neurones répondant au chaud et au froid (GRD, moelle épinière, thalamus, cortex). Les flèches indiquent la direction du flux d’information thermique.
Référence
Mario Carta 1#, Mikkel Vestergaard 2# & James. F. A Poulet 3,4#
The neuronal circuits and cellular encoding of thermosensation.
1 Institut Interdisciplinaire de Neurosciences, CNRS UMR 5297, Université de Bordeaux, Bordeaux 33000, France
2 Department of Neuroscience, Faculty of Health and Medical Sciences, University of Copenhagen, Copenhagen, Denmark.
3 Max Delbrück Center for Molecular Medicine in the Helmholtz Association (MDC), Berlin, Germany.
4 Neuroscience Research Center, Charité-Universitätsmedizin Berlin, Berlin, Germany.
# : Corresponding authors
DOI: 10.1038/s41583-025-01001-5
Mise à jour: 01/04/26
